|
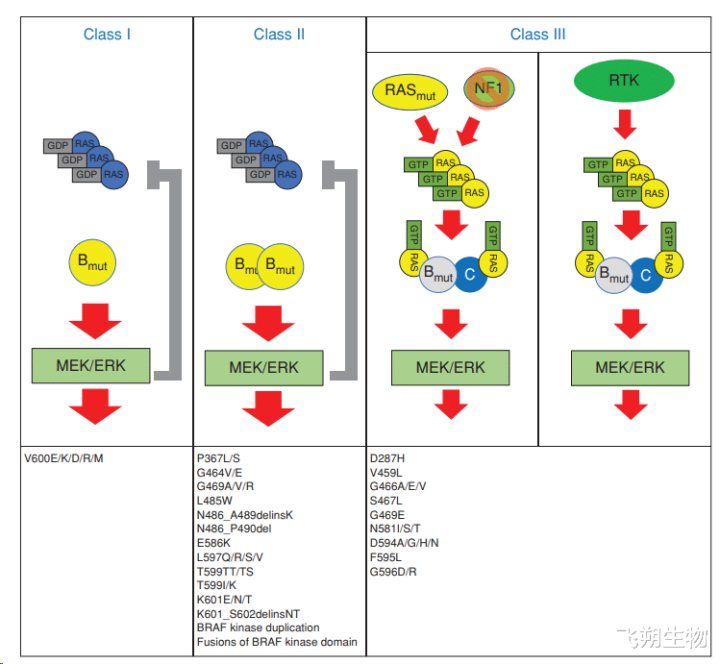
BRAF基因的生物学基础 RAF眷属卵白是一类丝氨酸/苏氨酸卵白激酶,其被视为促分裂素原活化蛋激酶(itogen-activated protein kinases , MAPK)信号通路的要津分子,在细胞滋长、分化和存活方面发达迫切作用。RAF眷属卵白有3种类型:A-RAF、B-RAF和C-RAF。MAPK通路转化使细胞增殖、滋长、分化和凋一火总计经过能够胜利进行;在这个信号通路中,小G卵白与RAF亚型的N-终局相联贯,从而活化RAF,RAF的活化导致卑劣MEK1、MEK2的磷酸化以及ERK1和ERK2的磷酸化,从而影响肿瘤细胞的增殖和细胞骨架的教导。 BRAF基因包含18个外显子,长约190kb,转录的mRNA长2.5kb,编码卵白质含783个氨基酸,相对分子量为94~95KDa。 把柄BRAF变异后激活功能是否依赖RAS分子和二聚化步地将BRAF变异分为三类:I类变异是指发生V600E/K/R/D等变异,不依赖RAS和二聚体作用,是作用最强的变异:II类变异曲直V600的变异,不依赖RAS分子,但需要与CRAF酿成二聚体而活化,具有中等强度的激酶活性:III类变异亦曲直V600变异但突变后使BRAF激酶功能缺失,依赖RAS和CRAF传递信号,激酶活性相对弱些。
BRAF基因突变类型[1] 肿瘤细胞中BRAF V600突变是最常见的变异步地,其中BRAF V600D/E/K/R是Ⅰ类突变,它们使BRAF激酶处于强活化情状,从而激活MAPK通路,其中V600E是最常见的突变,占BRAF V600突变的90%以上。
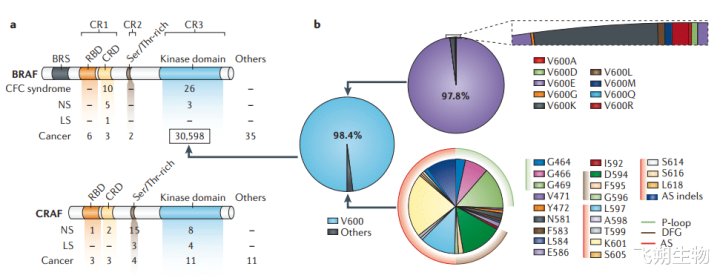
BRAF基因变异步地[2]
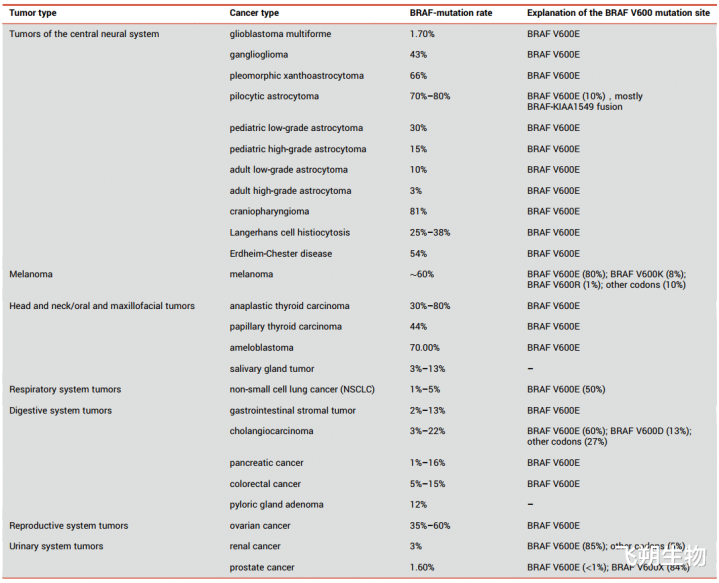
BRAF突变固然在多半肿瘤中都有,但是在四大癌种的突变频率相比高(玄色素瘤、甲状腺乳头状癌、结直肠癌、非小细胞肺癌主若是肺腺癌),其他癌种的省略突变频率不才表。
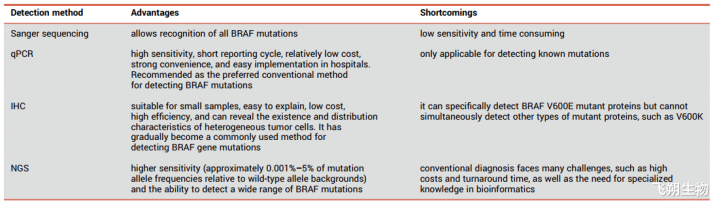
泛癌组织BRAF变异频率[3] BRAF的检测 现在,检测BRAF突变的主流表率包括多重逆转录团员酶链反馈(RT-PCR)、二代测序(NGS)、Sanger测序和免疫组化(IHC)等。有商议者远隔使用Sanger测序、多重RT-PCR、NGS,3种检测表率对138例NSCLC肿瘤组织样本进行平行检测,扫尾裸露,多重RT-PCR和NGS检测表率的奢睿度和准确性均高于Sanger测序,且多重RT-PCR和NGS检测裸表示相似的奢睿度和特异度澳门六合彩官网,检测扫尾具有高度一致性。因此NGS普及率高的癌种更优先保举NGS进行联检。
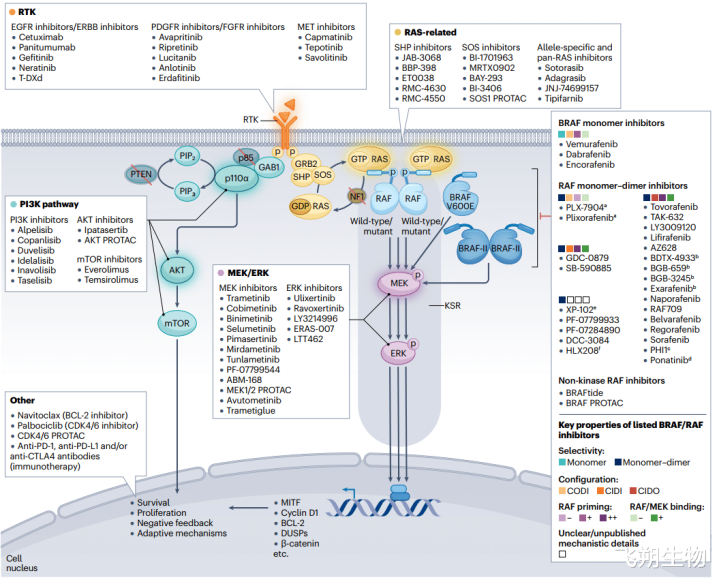
不同检测表率学对比[3] BRAF抑止剂 BRAF仍是被说明为是化合物可高度靶向的卵白,针对BRAF Ⅰ类突变研发的药物仍是获得一定的商议效果,BRAF抑止剂通过与BRAF突变单体的ATP部位相联贯,从而抑止卑劣的信号。MEK分为MEK1/2,可激活ERK,是RAS的卑劣应付因子,因此抑止MEK的活性不错阻断卑劣通路,进而齐备对上游基因变异引起的相配活化进行抑止。临床单用RAF或MEK抑止剂的患者中,约50%会在融合6~7个月后产生耐药[4]。从BRAF抑止剂在玄色素瘤中的获批到如今繁多的相宜症,以BRAF抑止剂为代表的靶向皆集疗法已成为多种BRAF突变阳性恶性实体肿瘤的主要融合妙技之一。
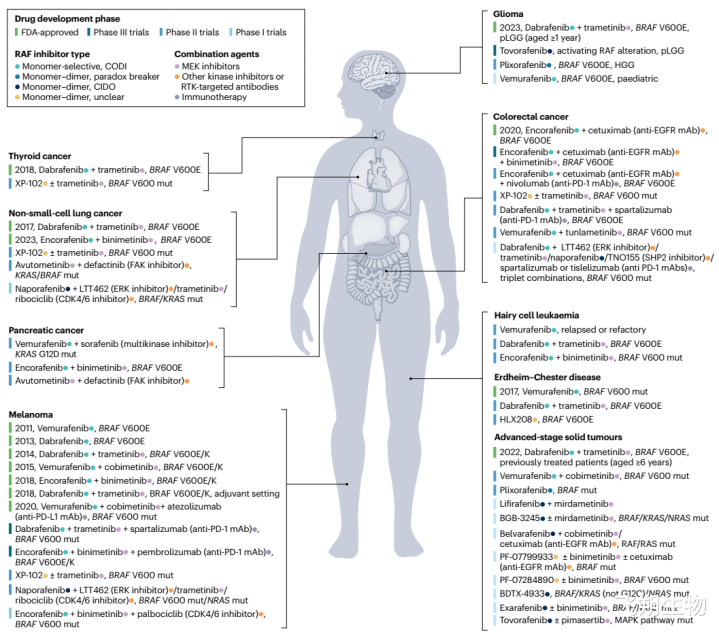
不同癌种BRAF抑止剂决策选用[5] BRAF突变在恶性实体肿瘤中的发病率及BRAF抑止剂在恶性实体肿瘤融合中获得的要津临床疗效如下[4]: (1)皮肤玄色素瘤中BRAF突变的发生率约为36.4%,BRAF抑止剂单药融合玄色素瘤的总生涯时候(overall survival,OS)达13.6个月,无进展生涯时候(progression free survival,PFS)达6.9个月,客不雅缓解率达48%;皆集MEK抑止剂OS达22.3~33.6个月,PFS达11.1~14.9个月,客不雅缓解率达63%~70%。 (2)乳头状甲状腺癌中BRAF突变的发生率为45%~50.9%,达拉非尼皆集曲好意思替尼OS为14.5个月,PFS为6.7个月,客不雅缓解率为56%。 (3)非小细胞肺癌中BRAF突变的发生率为3%,达拉非尼皆集曲好意思替尼PFS为9.0~14.6个月,ORR为63.2%~64%。 (4)结直肠癌中BRAF突变的发生率为6.5%~10.2%,康奈非尼皆集西妥昔单抗皆集或不皆集媲好意思替尼,其OS均为9.3个月,PFS为4.3~4.5个月,客不雅缓解率为20%~27%。 (5)BRAF突变也存在于核心神经系统肿瘤中,包括多形性黄色星形细胞瘤(56%)、胚胎发育不良性神经上皮肿瘤(3.4%)、神经节神经胶质瘤(40%)和毛细胞型星形细胞瘤(3.4%);达拉非尼皆集曲好意思替尼融合初级别胶质瘤的PFS为20.1个月,客不雅缓解率为46.6%。 (6)初级别浆液性卵巢癌中BRAF突变的发生率为2%~33%,达拉非尼皆集曲好意思替尼融合的客不雅缓解率为80%。 (7)胆说念癌中BRAF突变的发生率为1%~5%,达拉非尼皆集曲好意思替尼OS为13.5个月,PFS为9个月,客不雅缓解率达53%。 BRAF抑止剂融合耐药机制 有别于其他的激酶抑止剂,继发突变所致的耐药在BRAF较为稀有(举例L505H、L514V)。二代RAF抑止剂的耐药主要由促成二聚体的变异再行激活了ERK所致。这包括玄色素瘤中的NRAS突变、BRAF扩增和/或过抒发、BRAF剪接变异所指的RAS联贯区域丢失等。另外,旁路/卑劣信号通路的激活亦然耐药的成因之一。
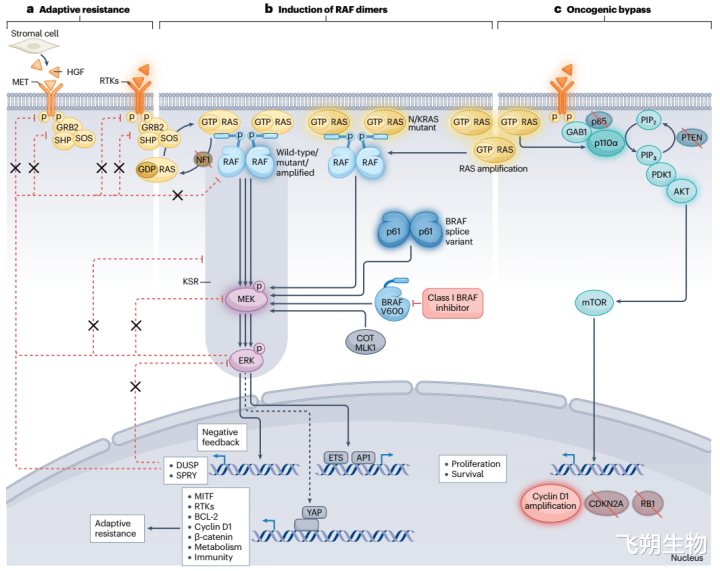
BRAF抑止剂耐药机制[5] 针对BRAF抑止剂耐药,可接头进行皆集用药,如与MEK抑止剂联用:BRAF抑止剂可使MEK通路激活,激发耐药。皆集MEK抑止剂能阻断该代偿性激活,如达拉非尼与曲好意思替尼皆集使用,可晋升疗效,减速耐药。与其他靶向药联用:如与PI3K/AKT/mTOR通路抑止剂联用,因该通路相配与BRAF抑止剂耐药算计,皆集用药可阻断旁路激活,克服耐药。与免疫融合药物联用:BRAF抑止剂会影响肿瘤微环境,与免疫融合药物如PD-1或PD-L1抑止剂联用,能增强免疫细胞对肿瘤细胞的识别和杀伤,晋升融合效果。 亦可竖立新一代BRAF抑止剂,竖立多靶点抑止剂:野心可同期抑止BRAF过火他相关耐药靶点的抑止剂,以更全面地阻断肿瘤细胞的信号传导,如能够同期抑止BRAF和MEK的双靶点抑止剂。优化抑止剂结构:通过对现存BRAF抑止剂的结构校正,晋升其与靶点的结协力和特异性,增强抑止效果,裁减耐药风险。
克服耐药机制战略[5] 回来 BRAF抑止剂已于多个癌种获批,以致可用于泛实体瘤的融合。但是BRAF复杂的分子机制导致现存的抑止剂难以克服耐药的问题,从而影响患者的临床结局。为进一步改善恶性肿瘤患者的临床结局,多种新药和皆集融合战略正在研发中,一样与之相关的临床诊疗决策及检测工夫也在不停完善中。让BRAF手脚融合靶点的不错有更多冲破,为纷乱患者提供更佳的融合契机。 参考文件 Cancer Discov. 2019 Mar;9(3):329-341. Nat Rev Mol Cell Biol 2015 May;16(5):281-98. Innovation (Camb). 2024 Oct 18;5(6):100661. 中华医学会肿瘤学分会, 中国临床肿瘤学会陌生肿瘤委员会. BRAF抑止剂融合恶性实体肿瘤大家共鸣(2024版)[J]. 中华肿瘤杂志, 2024, 46(10): 919-929. DOI: 10.3760/cma.j.cn112152-20240409-00142. Nat Rev Clin Oncol. 2024 Mar;21(3):224-247.澳门六合彩官网 |

 澳门六合彩官网
澳门六合彩官网